NH3 là một trong những hợp ý hóa học vô cơ sở trọng nhập lịch trình Hóa trung học phổ thông. Vậy ví dụ NH3 là gì, công thức và tính hóa chất của NH3 ra sao, với những phần mềm và cách thức pha trộn NH3 nào? Trong nội dung bài viết sau đây, Marathon Education sẽ hỗ trợ những em trả lời toàn bộ những vướng mắc này.
>>> Xem thêm: Bazơ Là Gì? Lý Thuyết Về Tính Chất Hóa Học Của Bazơ
Bạn đang xem: nh3 là axit hay bazơ
>>> Xem thêm: Tính Chất Hóa Học Của Lưu Huỳnh, Cách Điều Chế Và Các Ứng Dụng
Công thức chất hóa học của NH3
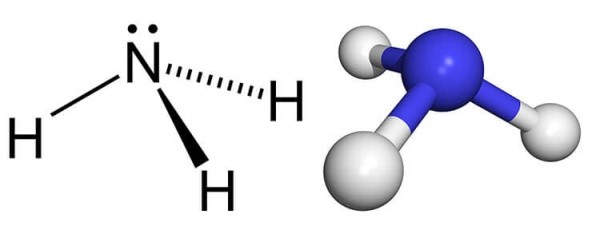
NH3 là công thức phân tử của Amoniac, thương hiệu này bắt mối cung cấp kể từ giờ đồng hồ Pháp và được thông ngôn đi ra giờ đồng hồ việt là a-mô-ni-ắc. Amoniac được cấu trúc kể từ 3 vẹn toàn tử Nitơ và 1 vẹn toàn tử Hidro tạo nên trở nên một hợp ý hóa học vô sinh với link kém cỏi bền.
Tính hóa chất của NH3
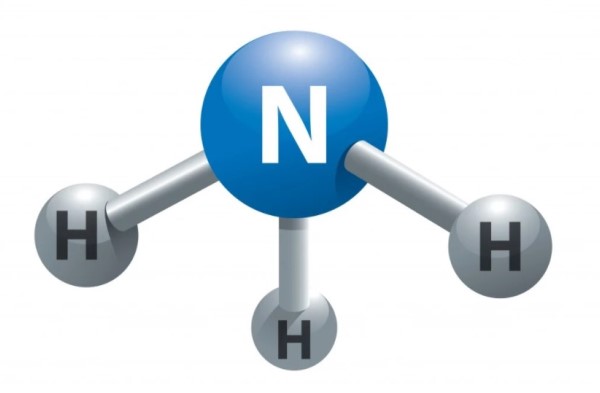
NH3 với tính bazơ yếu
Amoniac với tính bazơ yếu hèn, hỗn hợp amoniac với tài năng thực hiện quỳ tím hóa xanh lơ và thực hiện hỗn hợp phenolphtalein gửi lịch sự color hồng.
Nguyên nhân tạo nên tính bazơ yếu hèn của NH3 là vì cặp electron ko nhập cuộc link ở vẹn toàn tử N. Độ mạnh nhập tính bazơ của NH3 đối với một số trong những bazơ khác ví như sau:
Ba(OH)2 > NaOH > NH3 > Mg(OH)2 > Al(OH)3
Do với tính bazo nên amoniac hoàn toàn có thể phản xạ với nước, axit, hỗn hợp muối bột.
- Amoniac phản xạ với nước
NH3 + H2O ⇔ NH4+ + OH–
- Amoniac phản xạ với axit tạo nên trở nên muối bột amoni
NH3(khí) + HCl(khí) → NH4Cl(khói trắng)
NH3 + H2SO4 → NH4HSO4
2NH3 + H2SO4 → (NH4)2SO4
- Amoniac phản xạ với hỗn hợp muối bột (của những sắt kẽm kim loại tuy nhiên hidroxit ko tan) tạo nên trở nên bazơ và muối bột mới
2NH3+ MgCl2 + 2H2O → Mg(OH)2 + 2NH4Cl
3NH3 + AlCl3+ 3H2O →Al(OH)3↓ + 3NH4Cl
Chú ý: Khi tính năng với hỗn hợp muối bột của Cu2+, Ag+ và Zn2+, thành phầm chiếm được với kết tủa tiếp sau đó kết tủa tan tự tạo nên phức hóa học tan như: Cu(NH3)4(OH)2; Ag(NH3)2OH; Zn(NH3)4(OH)2.
Xem thêm: lời bài hát em gái mưa
ZnSO4+ 2NH3+ 2H2O → Zn(OH)2↓ + (NH4)2SO4
Zn(OH)2 + 4NH3 → [Zn(NH3)3](OH)2
NH3 với tính khử mạnh
Do Nitơ nhập NH3 với nấc lão hóa thấp nhất là -3 nên tiếp tục tạo nên hợp ý hóa học này còn có tính khử mạnh và vì vậy, NH3 với tài năng tính năng với Oxi, Clo và một số trong những oxit sắt kẽm kim loại không giống.
- Amoniac phản xạ với O2
4NH_3+3O_2\xrightarrow{t^o}2N_2\uparrow+6H_2O\\
4NH_3+5O_2\xrightarrow[Pt]{800^oC}4NO\uparrow+6H_2O
- Amoniac phản xạ với Cl2
2NH_3+3Cl_2\xrightarrow{t^o}N_2\uparrow+6HCl\\
8NH_3+3Cl_2\xrightarrow+N_2\uparrow+6NH_4Cl
- Amoniac phản xạ với oxit của kim loại
3CuO+2NH_3\xrightarrow{t^o}Cu+3H_2O+N_2\uparrow
NH3 với tài năng tạo nên phức
Như tiếp tục rằng, sự phối hợp những phân tử NH3 tự những electron ko dùng của vẹn toàn tử Nitơ với ion sắt kẽm kim loại đó là vẹn toàn tự tạo phức sau phản xạ.
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (màu xanh lơ thẫm)
AgCl + 2NH3 → [Ag(NH3)2]Cl
Tính hóa học cơ vật lý của NH3
- Trạng thái: NH3 tồn bên trên ở dạng khí, ko color, có mùi tanh không dễ chịu, với nồng khuôn khổ hoàn toàn có thể thực hiện nguy hại.
- Độ phân cực: Amoniac có tính phân đặc biệt rộng lớn tự phân tử NH3 với cặp electron tự tại và link N–H bị phân đặc biệt. Do vậy, amoniac là một trong những hóa học dễ dàng hóa lỏng.
- Độ hòa tan: NH3 vào vai trò là một trong những dung môi hòa tan chất lượng. NH3 có tài năng hòa tan những dung môi cơ học dễ dàng rộng lớn nước (do Amoniac với hằng số năng lượng điện môi nhỏ rộng lớn nước).

Phương pháp pha trộn NH3
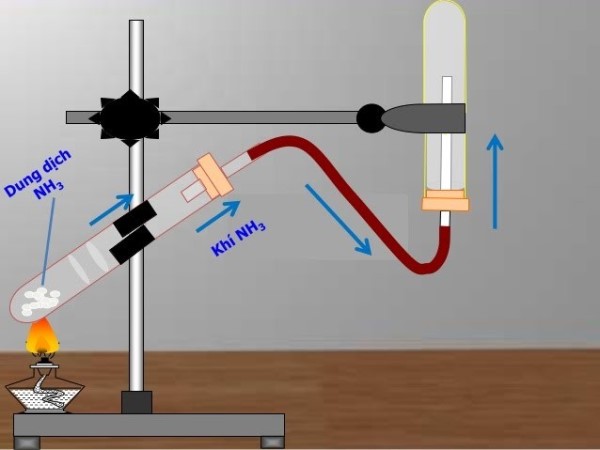
Trong chống thí nghiệm
Trong chống thực nghiệm, NH3 thông thường được pha trộn tự 2 cơ hội như sau:
- Cho muối bột amoni tính năng với hỗn hợp kiềm:
NH4Cl + NaOH → NaCl + NH3 + H2O
- Nhiệt phân muối bột amoni
NH_4Cl\xrightarrow{t^o}NH_3+HCl\\
NH_4HCO_3\xrightarrow{t^o}NH_3+H_2O+CO_2
Trong công nghiệp
Trong công nghiệp, NH3 được tổ hợp kể từ N2và H2:
N_2+3H_2\xrightarrow[Fe]{450^oC,\ p}2NH_3
Ứng dụng của NH3

Amoniac được phần mềm nhiều cho tới phát hành và cuộc sống trong số nghành nghề thịnh hành như:
Dùng thực hiện phân bón
Hầu không còn lượng Nitơ đều phải có xuất xứ kể từ NH3, đặc biệt quan trọng cho việc trở nên tân tiến của cây xanh vì vậy tuy nhiên bên trên thực tiễn có tầm khoảng 83% amoniac lỏng được sử dụng thực hiện phân bón, hùn ngày càng tăng năng suất của cây xanh.
Xem thêm: trong quá trình dịch mã
Dùng thực hiện dung dịch tẩy
- Amoniac lỏng đưa đến khả năng chiếu sáng tỏa nắng rực rỡ và với tài năng tạo nên tẩy color, vì vậy nhập cuộc sống, hỗn hợp NH3 được dùng thực hiện hóa học tẩy cọ cho tới nhiều mặt phẳng.
- Ngoài đi ra, amoniac còn được dùng làm rửa sạch thủy tinh ma, vật dụng sứ và thép ko han, rửa sạch đồ đạc và vật dụng dính bụi,…
Dùng nhằm xử lý khí thải
Trong xử lý khí thải, amoniac lỏng được phần mềm nhằm mục tiêu vô hiệu hóa những hóa học như Nox, Sox. Các hóa học này còn có trong số loại khí thải khí nhen những nguyên vật liệu hóa thạch như than vãn, đá…
Dùng nhập công nghiệp (dệt may, thức ăn, dầu khí, khai quật gỗ…)
- Trong công nghiệp, amoniac được phần mềm nhiều trong số ngành công nghiệp như tết may, thức ăn, dầu khí, khai quật mộc,… Amoniac lỏng sử dụng tết vải vóc, đưa đến hóa học kiềm bóng.
- Do với tính khử mạnh, Amoniac khan được dùng làm hạn chế hoặc vô hiệu hóa nhiễm trùng của thịt trườn hiệu suất cao.
- Amoniac phản xạ với color ngẫu nhiên nhập mộc và thực hiện thay cho thay đổi sắc tố. Do vậy, bọn chúng được phần mềm nhập phát hành mộc thực hiện sắc tố của mộc trở thành đậm rộng lớn.
- Trong công nghiệp dầu khí, amoniac được sử dụng thực hiện hóa học hòa hợp axit, bộ phận của dầu thô và có công năng bảo đảm những khí giới không bị bào mòn.
- Trong khai quật mỏ, NH3 được dùng nhằm khai quật những sắt kẽm kim loại như đồng, niken và molypden,…
Tham khảo tức thì những khoá học tập online của Marathon Education
Qua nội dung bài viết bên trên hẳn những em tiếp tục cầm được tính hóa chất của NH3 cũng tựa như các kiến thức và kỹ năng tương quan về đặc thù cơ vật lý, cơ hội pha trộn, ứng dụng… Để học tập thêm thắt nhiều kiến thức và kỹ năng Toán Lý Hóa có lợi không giống, những em hãy theo dõi dõi trang web Marathon Education. Chúc những em luôn luôn tiếp thu kiến thức chất lượng và đạt điểm cao!
Hãy tương tác tức thì với Marathon sẽ được tư vấn nếu như những em mong muốn học online trực tuyến nâng lên kiến thức và kỹ năng nhé! Marathon Education chúc những em được điểm trên cao trong số bài xích đánh giá và kỳ ganh đua chuẩn bị tới!











Bình luận