Nồng chừng mol là gì, bao gồm những dạng bài bác luyện cần thiết, thông thường gặp gỡ nhập lịch trình chất hóa học trung học tập. Vậy nó được xem như vậy nào? Hãy nằm trong VietChem lần hiểu cụ thể nhập nội dung bài viết sau và tìm hiểu thêm một vài bài bác luyện áp dụng nhằm làm rõ rộng lớn nhé.
Nồng chừng mol là gì?
Nồng chừng mol biểu thị mang lại số mol của một hóa học tan nhập một lít dụng dịch, nó được kí hiệu là M
Bạn đang xem: các công thức tính số mol
Ví dụ: Trong 4 lít hỗn hợp chứa chấp 2 mol phân tử tan tạo ra hỗn hợp 0,5 M hoặc hay còn gọi là 0,5 phân tử gam.
Ngày ni mol được sử dụng thoáng rộng nhập chất hóa học nhằm thể hiện tại lượng hóa học phản xạ nằm trong thành phầm của những phản xạ học tập. Bên cạnh đó, nó còn được dùng nhằm biểu thị con số vẹn toàn tử, những thực thể không giống nhau nhập một kiểu mẫu chắc chắn của một hóa học hoặc ion.

Nồng chừng mol là gì
>>>XEM THÊM: Chất thải nguy nan sợ hãi - Phân loại, mã color quy tấp tểnh và cơ hội xử lý
Chất thải nguy nan sợ hãi - Phân loại, mã color quy tấp tểnh và cơ hội xử lý
Công thức tính mật độ mol
- Ta đem công thức:
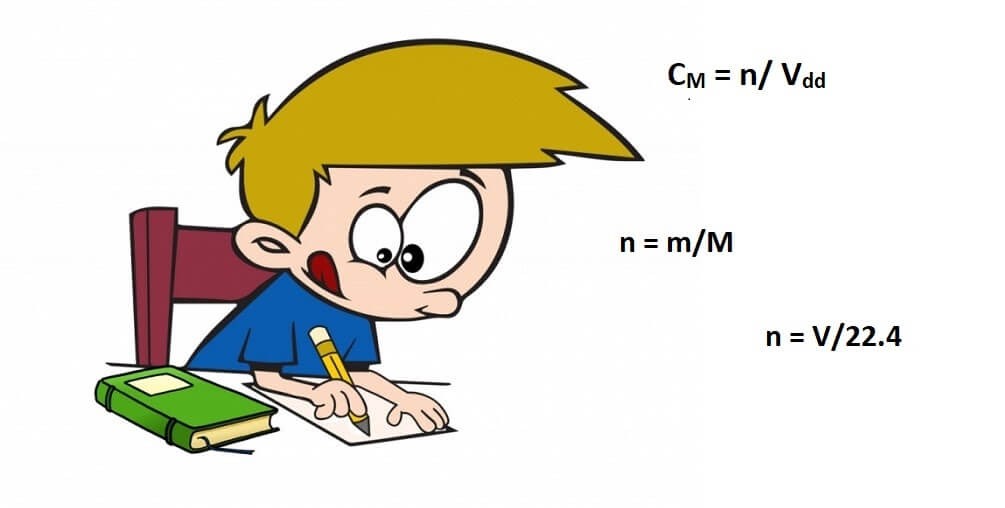
CM = n/ Vdd
Trong đó:
- CM là mật độ mol
- n là số mol hóa học tan
- Vdd là thể tích hỗn hợp (đơn vị tính: lít)
Công thức tính số mol đơn giản
1. Cách tính số mol qua chuyện thể tích
n = V/22.4
Trong đó:
- n là số mol hóa học khí bên trên ĐK chi phí chuẩn chỉnh (đktc) với đơn vị chức năng tính: mol
- V: thể tích của hóa học khí ở đktc (tính vì như thế lít)
2. Tính số mol trải qua khối lượng
n = m/M
Trong đó:
- n là số mol, đem đơn vị chức năng tính là mol
- m là lượng được xem vì như thế gam
- M là lượng mol hóa học, tính vì như thế g/mol
3. Một số phương pháp tính khác
|
Điều kiện |
Công thức |
Chú thích |
Đơn vị tính |
|
Khi đem mật độ mol/lít |
n = CM.V |
- n: số mol chất |
mol |
|
- CM: mật độ mol |
Mol/lit |
||
|
- V: thể tích dung dịch |
lit |
||
|
Khi biết số vẹn toàn tử hoặc phân tử |
n = A/N |
- A: số vẹn toàn tử hoặc phân tử |
Nguyên tử hoặc phân tử |
|
- Số Avogadro (số đơn vị chức năng nhập bất kể một mol hóa học này và có mức giá trị vì như thế 6.1023) Xem thêm: làm tròn đến hàng đơn vị |
|||
|
Tính số mol khí bên trên ĐK thường |
n = Phường.V/R.T |
- P: gí suất |
1 atm = 760mmHg |
|
- V: thể tích khí |
Lít |
||
|
- R: hằng số |
0,082 (hoặc 62400) |
||
|
- T: nhiệt độ chừng tính theo dõi chừng Kelvin (K) |
K = 273 + chừng C |

Có rất rất nhiều phương pháp tính số mol
Tham khảo một vài bài bác thói quen mật độ mol
Một số bài bác luyện tìm hiểu thêm về kiểu cách tính mật độ mol:
Bài luyện 1: Trong 400ml hỗn hợp đem hòa tan 32 gam hóa học NaOH. Hãy tính mật độ mol của dung dịch
Lời giải:
- Đổi 400 ml = 0,4 lít
- nNaOH = 36/40 = 0,9 mol
- Theo công thức tính CM tao có:
- Cdd = n/V = 0,9/0,4 = 2,25 (M)
Bài luyện 2: Tính CM của 0,5 mol MgCl2 đem trong một,5 lít dung dịch
Lời giải:
- Áp dụng nhập công thức tính CM tao có:
CM = 0,51 x 5 = 0,33 (mol)
Bài luyện 3: Tính mật độ mol của một hỗn hợp chứa chấp 0,5 mol NaCl nhập 5 lít hỗn hợp.
Lời giải:
CM = 0,5/5 = 0,1 (mol)
Bài luyện 4: Hãy tính mật độ mol của hỗn hợp Lúc tổ chức hòa tan 15,8g KMnO4 nhập 7,2 lít nước.
Lời giải:
- Số mol của hóa học nKMnO4 là:
nKMnO4 = 15,8/ 158 = 0,1 (mol)
- Vậy CM tiếp tục bằng: 0,1/ 7,2 = 0,0139
Bài luyện 5: Tiến hành mang lại 6,5 gam kẽm phản xạ một vừa hai phải đầy đủ với 100 ml hỗn hợp axit chohidric (HCl). Hãy:
- a) Tính thể tích của H2 chiếm được ở ĐK chi phí chuẩn
- b) Tính mật độ mol của hỗn hợp HCl tiếp tục sử dụng
Lời giải:
Xem thêm: ở đậu hà lan gen a quy định hạt vàng
- Theo bài bác đi ra tao có:
nZn = 6,5/ 65 = 0,1 mol
- Phương trình phản ứng:
Zn + 2HCl → ZnCl2 + H2
- nZn = nZnCl2 = 0,1 mol
- nHCl = 2nZn = 0,2 mol
- a) VH2 = 0,1 x 22,4 = 2,24 (lít)
- b) CddHCl = 0,2/ 0,1 = 2 (M)
Trên trên đây, VietChem tiếp tục trình làng cho chính mình gọi cụ thể về nồng chừng mol là gì gần giống phương pháp tính và một vài bài bác luyện áp dụng cơ bạn dạng. Mong rằng, qua chuyện nội dung bài viết tiếp tục giúp đỡ bạn làm rõ rộng lớn những yếu tố này và rất có thể vận dụng nhập học hành hoặc việc làm. Truy cập anhnguucchau.edu.vn thông thường xuyên để tiếp gọi nhiều nội dung bài viết hữu ích không giống.





.png)






Bình luận